|

高效活性药物成分(HPAPI)、大分子(生物制剂)药物以及无菌灌装与后续工艺需要采用隔离且无菌的生产环境。气化过氧化氢(H2O2)是隔离制药生产中杀菌的主要处理方法。如果在杀菌和通风后或在生产流程中的任何阶段残留的H2O2 水平过高,药物产品就会发生氧化和降解。这不仅代价昂贵,还可能影响药物的安全性。
制药生产的 H2O2 水平
美国职业安全与健康研究所(NIOSH)在29CFR 1900 中规定一般工业工人对 H2O2 的建议接触限值(REL)为百万分之一(ppm)。其它适用标准可能因特定工业和接触时间而有所不同,但它们通常在ppm 范围内。虽然对人类的健康和安全来说已经足够,但 ppm 的水平仍然过高,无法防止药物氧化,也无法维持药物效能、安全性和稳定性。美国食品和药物管理局(FDA)要求在使用 H2O2 进行灭菌的隔离应用中,最大残留水平为 100 ppb。
药物中过氧化氢的残留在100ng/ml,就需要考虑药物被氧化活性降低的可能了(more viewpoints and demonstrations prove that the acceptable H2O2 uptake level was determined to be 100 ng/mL for the antibody in the H2O2 spiking study; protein oxidation was observed above this threshold.)
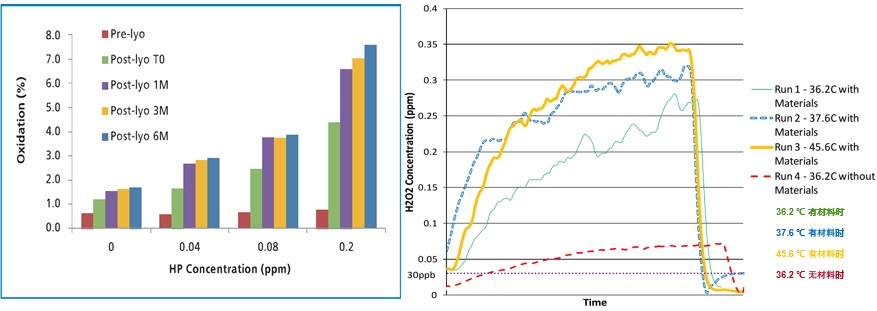
隔离器中众多塑料材质对过氧化氢吸附效应,导致过氧化氢残留持续存在;

其中过氧化氢吸附能力:POM>硅胶>CSM>PVC>PE,因此我们需要考虑审慎对待塑料材质在隔离器中的应用!
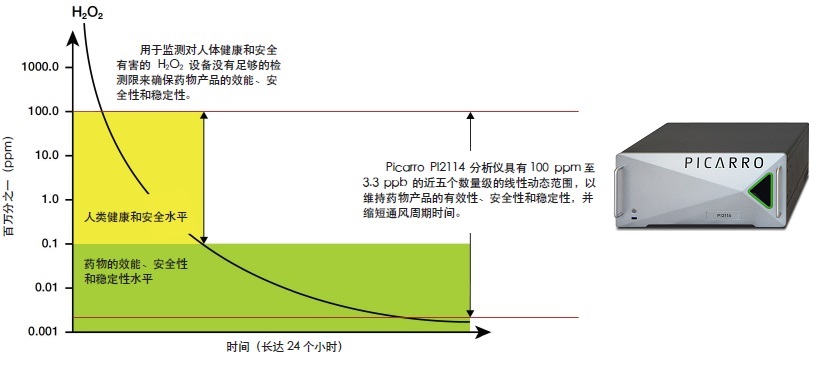
Picarro公司的ppb级别的过氧化氢检测仪
Picarro PI2114 气体浓度分析仪提供了从100 ppm 至 3.3 ppb 的 H2O2 持续监测,精度为 1.1 ppb; Picarro PI2114 分析仪确保了过氧化氢的超低残留水平,以帮助避免药物被氧化,并保障了GMP制药生产应用中药物的效能、安全性和稳定性,其中包括高效原料药(API)和生物制剂的生产以及无菌灌装与后续工艺;
PI2114 性能:
连续实时的 H2O2 监测
3.3 ppb 检测下限
1.1 ppb 精度
< 1分钟的响应时间 |
GMP合规:
美国食品和药品管理局 21CFR Part11
安装确认(IQ)和操作确认(OQ)
快速、简易的性能验证方法 |
以下特点可节省成本:
无需湿化学品或消耗品
没有活动组件,无需频繁维护
长期稳定性,无需频繁校准 |
|
